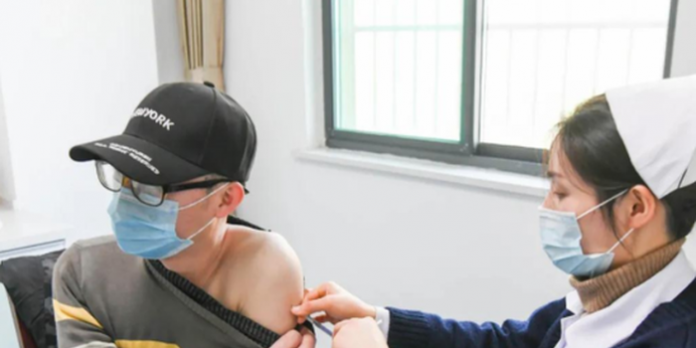
【华闻】雅加达讯。中国一种新的疫苗正在印尼进行第三阶段的临床试验。这是由中国科学院微生物研究所和安徽智飞龙科马生物制药有限公司联合研发的重组新型冠状病毒疫苗(CHO细胞),自今年三月份经中国国家卫生健康委提出建议,国家药监局组织论证同意紧急使用。这疫苗一般被称为安徽疫苗。
据万隆巴查查兰Padjadjaran(Unpad)大学的安徽新冠重组疫苗第三阶段临床试验小组发言人穆哈默法伊沙(Muhammad Faisal)日前对媒体说,巴查查兰大学医学院研发小组已对中国的安徽疫苗进入了第三阶段临床试验。
这项临床试验在万隆的6个医院地点进行,涉及约2,000名志愿者,在雅加达也有相同数量的志愿者。
据英国广播公司BBC周五(16/4)报道,安徽新冠疫苗是由安徽智飞隆康生物制药公司开发的,该公司还正在为印尼朝圣或朝觐者开发脑膜炎疫苗。安徽疫苗临床试验由印尼BCHT Biotechnology公司赞助,那是安徽省的外国投资公司。
在此之前,安徽疫苗已经在中国通过了第一阶段和第二阶段的临床试验。第一阶段涉及50名志愿者,第二阶段涉及900志愿者。
“根据我们在第1阶段和第2阶段获得的总结报告,这种重组疫苗是安全的。但是,与其他疫苗一样,每个人可能会有反应或出现免疫后续事件的副作用(AEFI),出现局部反应,可能是全身反应。对于局部症状,与其他疫苗一样,注射部位出现瘙痒和疼痛,或全身发烧或头晕。“
重组疫苗第III阶段临床试验的主要研究员罗德曼Rodman Tarigan医生说,安徽重组疫苗的第一和第二阶段临床试验结果被认为是安全的,并具有出色的免疫力。
。在III阶段临床试验中,研究小组将确定安徽疫苗的疗效水平。
他说:“我们希望安徽疫苗的疗效将超过世界卫生组织的阈值,超过50%。”
罗德曼医生还说,安徽疫苗具有超越其他疫苗的优势。
“与使用腺病毒载体疫苗和灭活疫苗形式的疫苗对比。基于新冠病毒的尖峰糖蛋白(蛋白S)平台的重组疫苗,理论上可以触发更高抗体的形成并能够提供更全面的保护。”
根据巴查查兰大学官方网站的报告,临床试验将持续12到14个月。所涉及的志愿者将每三个月注射一次疫苗或安慰剂,每次间隔三个月。同时在临床试验期间监测病情。
稍后,临床试验结果将报告给药物与食品监督机构BPOM,用作发布紧急使用授权(EUA)的考虑因素。预计EUA最早将于2021年9月发布。(p/int)
Kabar Terbaru Vaksin Anhui, Kini Uji Klinis Fase III